의약품 제조업체: Bioverativ Therapeutics Inc. (Updated: 2023-05-05)
처방 정보 하이라이트
ELOCTATE® [Antihemophilic factor (recombinant), Fc fusion protein], 동결건조 분말 주사용 용액
미국 최초 승인: 2014
적응증 및 용법
ELOCTATE, Antihemophilic Factor (Recombinant), Fc Fusion Protein은 성인 및 소아의 A형 혈우병(선천성 제VIII 인자 결핍) 환자에서 다음과 같은 경우에 사용되는 재조합 DNA 유래 항혈우병 인자입니다.
- 출혈 에피소드의 주문형 치료 및 관리
- 수술 전후 출혈 관리
- 출혈 에피소드의 빈도를 줄이기 위한 일상적인 예방
사용 제한
ELOCTATE는 폰 빌레브란트병 치료에 사용하도록 승인되지 않았습니다. (1)
용량 및 투여
재구성 후 정맥 주입용으로만 사용하십시오.
- 각 바이알의 ELOCTATE에는 재조합 제VIII 인자의 양이 국제 단위(IU 또는 단위)로 표시되어 있습니다. 체중 킬로그램당 1단위는 제VIII 인자 수치를 2%(IU/dL) 증가시킵니다. (2.1)
- 출혈 에피소드의 주문형 치료 및 관리 및 수술 전후 관리의 경우 다음 공식을 사용하여 용량을 계산합니다.
제VIII 인자의 예상 증가량(IU/dL 또는 정상 비율) = [총 용량(IU)/체중(kg)] x 2(IU/dL/IU/kg)
또는
필요한 용량(IU) = 체중(kg) x 원하는 제VIII 인자 증가량(IU/dL 또는 정상 비율) x 0.5(IU/kg/IU/dL) - 일상적인 예방의 경우: 4일마다 50IU/kg. 3~5일 간격으로 25~65IU/kg 범위에서 투여하면서 환자 반응에 따라 용량을 조정합니다.
- 6세 미만 소아의 일상적인 예방의 경우: 주 2회 50IU/kg. 3~5일 간격으로 25~65IU/kg 범위에서 투여하면서 환자 반응에 따라 용량을 조정합니다. 최대 80IU/kg의 더 빈번하거나 더 높은 용량이 필요할 수 있습니다. (2.1)
투여 형태 및 함량
주사용: 명목상 250, 500, 750, 1000, 1500, 2000, 3000, 4000, 5000 또는 6000IU, 재구성을 위한 단회 투여용 바이알에 든 동결건조 분말. (3)
금기
ELOCTATE 또는 ELOCTATE의 부형제(수크로오스, 염화나트륨, L-히스티딘, 염화칼슘 및 폴리소르베이트 20)에 대해 아나필락시스를 포함한 생명을 위협하는 과민성 반응을 경험한 적이 있는 환자에게는 사용하지 마십시오. (4)
경고 및 주의사항
이상 반응
이전에 치료받은 환자(PTP): 임상 시험에서 가장 흔하게 발생한 이상 반응(대상의 >0.5%)은 관절통, 권태감, 근육통, 두통 및 발진이었습니다. (6)
이전에 치료받지 않은 환자(PUP): 임상 시험에서 가장 흔하게 발생한 이상 반응(발생률 ≥1%)은 제VIII 인자 억제, 기기 관련 혈전증 및 구진성 발진이었습니다. (6)
의심되는 이상 반응을 보고하려면 Bioverativ Therapeutics Inc.(1-855-693-5628) 또는 FDA(1-800-FDA-1088 또는 www.fda.gov/medwatch)에 문의하십시오.
환자 상담 정보 및 FDA 승인 환자 라벨링은 17을 참조하십시오.
개정일: 2023년 5월
목차
전문 정보: 내용*
1 적응증 및 사용법
2 용법 및 용량
2.1 용량
2.2 조제 및 재구성
2.3 투여
3 제형 및 강도
4 금기 사항
5 경고 및 주의 사항
5.1 과민 반응
5.2 중화 항체
5.3 심혈관 위험 요인
5.4 카테터 관련 합병증
5.5 실험실 검사 모니터링
6 이상 반응
6.1 임상 시험 경험
6.2 시판 후 경험
8 특정 인구 집단에서의 사용
8.1 임신
8.2 수유
8.4 소아 사용
8.5 노인 사용
11 설명
12 약리학
12.1 작용 기전
12.2 약력학
12.3 약동학
13 비임상 독성학
13.1 발암성, 돌연변이 유발성, 생식 능력 손상
14 임상 연구
15 참고 문헌
16 포장 단위/보관 및 취급
17 환자 상담 정보
- *
- 전문 정보에서 생략된 섹션 또는 하위 섹션은 나열되지 않습니다.
1. 적응증 및 용법
ELOCTATE, Antihemophilic Factor (Recombinant), Fc Fusion Protein은 재조합 DNA 유래 항혈우병 인자로, 성인 및 소아의 혈우병 A (선천성 제VIII 인자 결핍) 환자에서 다음과 같은 경우에 사용됩니다.
- 출혈 에피소드의 주문형 치료 및 관리
- 수술 전후 출혈 관리
- 출혈 에피소드 빈도 감소를 위한 일상적 예방
사용 제한
ELOCTATE는 폰 빌레브란트병 치료에 사용되지 않습니다.
2. 용법 및 용량
재구성 후 정맥 주사만 가능합니다.
2.1 용량
- 투여 용량 및 치료 기간은 VIII 인자 결핍의 중증도, 출혈 부위 및 범위, 환자의 임상 상태에 따라 달라집니다. 주요 수술 또는 생명을 위협하는 출혈 발생 시 대체 요법을 주의 깊게 모니터링해야 합니다.
- ELOCTATE의 각 바이알 라벨에는 국제 단위(IU)로 VIII 인자 역가가 표시되어 있습니다. 1IU는 정상 인간 혈장 1밀리리터에 포함된 VIII 인자의 활성에 해당합니다.
- 역가 지정은 크로모젠 기질 분석법을 사용하여 결정됩니다. 현장 연구1에 따르면 혈장 VIII 인자 수준은 미국 임상 실험실에서 일반적으로 사용되는 크로모젠 기질 분석법 또는 단일 단계 응고 분석법을 사용하여 모니터링할 수 있습니다.
- 필요한 VIII 인자 용량 계산은 체중 1kg당 VIII 인자 1IU가 혈장 VIII 인자 수준을 2IU/dL 증가시킨다는 경험적 발견에 기반합니다.
IU/dL(또는 정상의 %)로 표현된 VIII 인자 수준의 예상 in vivo 최고 증가량은 다음 공식을 사용하여 추정됩니다.
VIII 인자 증가량 추정치(IU/dL 또는 정상의 %) = [총 용량(IU)/체중(kg)] × 2(IU/kg당 IU/dL)
원하는 in vivo VIII 인자 수준 최고 증가량을 달성하기 위한 용량은 다음 공식을 사용하여 계산할 수 있습니다.
용량(IU) = 체중(kg) × 원하는 VIII 인자 증가량(IU/dL 또는 정상의 %) × 0.5(IU/dL당 IU/kg)
- 환자는 약동학적(예: 반감기, in vivo 회복) 및 임상 반응이 다를 수 있습니다. ELOCTATE의 용량 및 빈도는 개별 임상 반응에 따라 결정합니다.
- 6세 미만의 소아 환자의 경우 용량 조절이 필요할 수 있습니다 [특정 인구 집단에서의 사용(8.4) 참조]. 6세 이상의 환자의 경우 일반적으로 용량 조절이 필요하지 않습니다.
요청 시 치료 및 출혈 발생 조절
요청 시 치료 및 출혈 발생 조절을 위한 ELOCTATE 투여에 대한 지침은 표 1에 나와 있습니다. VIII 인자 활성을 목표 범위 이상으로 유지하는 것을 고려해야 합니다.
| 출혈 유형 | 필요한 VIII 인자 수준 (IU/dL 또는 정상의 %) |
용량 (IU/kg) |
투여 빈도(시간) | 치료 기간(일) |
|---|---|---|---|---|
| 경미 및 중등도 관절, 표재성 근육/신경혈관 손상 없음(장골근 제외), 심층 열상 및 신장, 표재성 연조직, 점막 |
40-60 | 20-30 | 24-48시간마다 반복 (6세 미만 환자의 경우 12~24시간) |
출혈 발생이 해결될 때까지 |
| 중증 생명 또는 사지 위협적인 출혈, 장골근 및 신경혈관 손상이 있는 심층 근육, 복막 후, 두개내 또는 위장관 |
80-100 | 40-50 | 12~24시간마다 반복(6세 미만 환자의 경우 8~24시간) | 출혈이 해결될 때까지 (약 7~10일) |
수술 전후 관리
수술 중 ELOCTATE 투여에 대한 지침(수술 전후 관리)은 표 2에 나와 있습니다. 표적 범위 이상의 VIII 인자 활성을 유지하는 것을 고려해야 합니다.
| 수술 유형 | 필요한 VIII 인자 수치 (IU/dL 또는 정상의 %) |
투여량 (IU/kg) |
투여 빈도 (시간) |
치료 기간(일) |
|---|---|---|---|---|
| 경미한 합병증 없는 치아 발치 |
50-80 | 25-40 | 24시간마다 반복(6세 미만 환자의 경우 12-24시간) | 치유가 될 때까지 최소 1일 |
| 중증 두개내, 복강내 또는 관절 치환 수술 |
80-120 (수술 전후) |
수술 전: 40-60 반복: 40-50 |
40~60 IU/kg의 수술 전 투여 후 8~24시간(6세 미만 환자의 경우 6~24시간) 후에 40~50 IU/kg의 반복 투여를 하고, 그 후 FVIII 활성을 표적 범위 내로 유지하기 위해 24시간마다 반복 투여 | 적절한 상처 치유가 될 때까지, 그 후 FVIII 활성을 표적 범위 내로 유지하기 위해 최소 7일 동안 치료를 계속 |
일상적인 예방
- 권장 시작 요법은 4일마다 50 IU/kg의 ELOCTATE를 투여하는 것입니다. 3-5일 간격으로 25-65 IU/kg 범위의 투여량으로 환자의 반응에 따라 요법을 조정합니다.
- 6세 미만의 어린이의 경우 권장 시작 요법은 일주일에 두 번 50 IU/kg의 ELOCTATE를 투여하는 것입니다. 3-5일 간격으로 25-65 IU/kg 범위의 투여량으로 환자의 반응에 따라 요법을 조정합니다. 80 IU/kg까지 더 빈번하거나 더 높은 투여량이 필요할 수 있습니다 [특정 인구 집단에서의 사용 (8.4), 임상 약리학 (12.3) 참조].
2.2 준비 및 재구성
- 재구성 절차 중에는 무균 기법(깨끗하고 무균)과 평평한 작업 표면을 사용하십시오.
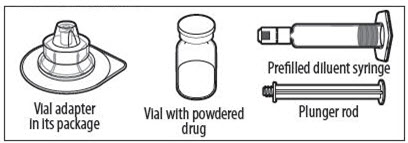
- 흰색에서 벗어난 흰색의 동결 건조 분말이 들어 있는 ELOCTATE 바이알과 미리 채워진 희석제 주사기를 사용하기 전에 실온에 도달하도록 하십시오.
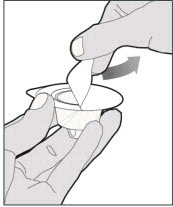
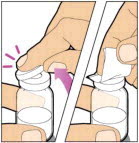
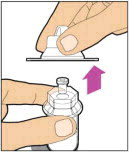
- 바이알에서 플라스틱 캡을 제거하고 알코올 솜으로 바이알의 고무 마개를 닦으십시오. 고무 마개가 마르도록 하십시오.
-
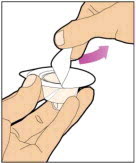
바이알 어댑터 포장에서 뚜껑을 벗겨 바이알 어댑터 포장에서 완전히 제거하십시오. 바이알 어댑터를 포장에서 제거하거나 어댑터 포장의 내부를 만지지 마십시오.
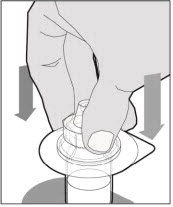
-
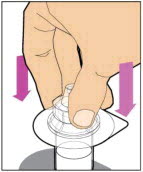
바이알을 평평하고 단단한 표면에 놓고 한 손으로 바이알을 고정하십시오. 다른 손으로 바이알 어댑터를 바이알 위에 놓습니다. 어댑터 스파이크를 고무 마개 중앙 바로 위에 놓고 스파이크가 바이알 마개 중앙을 관통하고 완전히 삽입될 때까지 어댑터를 직접 아래로 누릅니다.
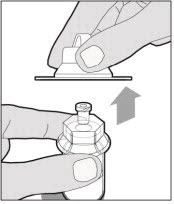
-
포장 덮개를 바이알 어댑터에서 들어올려 버립니다.
-
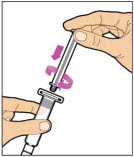
원형 디스크에서 플런저 로드를 잡습니다. 플런저 로드의 끝을 주사기 끝에 놓습니다. 단단히 고정될 때까지 시계 방향으로 돌립니다. ELOCTATE 포장에 제공된 희석제 주사기만 사용하십시오.
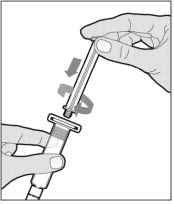
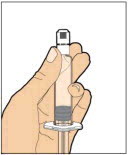
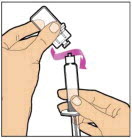
- 한 손으로 캡이 위로 향하도록 캡 바로 아래의 톱니 모양 부분을 잡고 희석제 주사기를 잡습니다. 캡이 제거되었거나 단단히 고정되지 않은 경우 사용하지 마십시오.
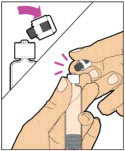
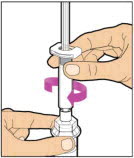
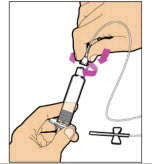
- 다른 손으로 캡을 잡고 90° 각도로 구부려 끊어집니다. 캡이 끊어지면 주사기의 유리 끝이 보입니다. 주사기의 유리 끝이나 캡의 내부를 만지지 마십시오.
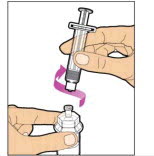
- 바이알을 평평한 표면에 놓고 주사기 끝을 어댑터 구멍에 삽입합니다. 어댑터에 단단히 고정될 때까지 주사기를 시계 방향으로 돌립니다.
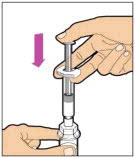
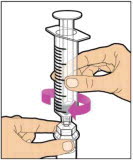
- 플런저 로드를 천천히 눌러 희석제를 모두 바이알에 주입합니다. 이 과정이 끝나면 플런저 로드가 약간 올라갈 수 있습니다. 이는 정상입니다.
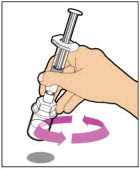
- 주사기가 어댑터에 연결된 상태로 제품이 완전히 용해될 때까지 바이알을 부드럽게 흔듭니다. 흔들지 마십시오. 재구성된 용액은 투명하거나 약간 불투명하고 무색이어야 합니다. 가시적인 입자가 있거나 흐린 경우 재구성된 ELOCTATE를 사용하지 마십시오.
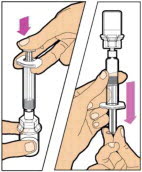
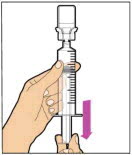
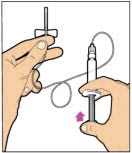
- 플런저 로드가 완전히 눌러졌는지 확인하십시오. 바이알을 거꾸로 뒤집습니다. 플런저 로드를 천천히 당겨 용액을 주사기로 흡입합니다. 플런저 로드가 주사기에서 완전히 빠져나오지 않도록 주의하십시오.
- 주사기를 바이알 어댑터에서 부드럽게 풀고 어댑터가 여전히 부착된 상태로 바이알을 버립니다. 주사기 끝이나 캡의 내부를 만지지 마십시오.
- 재구성된 ELOCTATE를 가능한 한 빨리 사용하십시오. 그러나 재구성 후 3시간 이내에 사용하십시오. 재구성 후 즉시 사용하지 않는 경우 주사기의 유리 끝을 만지지 마십시오. 직사광선을 피하십시오. 재구성 후 냉장 보관하지 마십시오.
ELOCTATE 바이알을 2개 이상 결합하려면 위의 12단계 후에 다음과 같은 풀링 단계를 따르십시오.
- 희석제 주사기를 바이알 어댑터에서 완전히 분리될 때까지 시계 반대 방향으로 돌려 제거합니다.
- 큰 루어 록 주사기(키트에 포함되지 않음)를 부착하는 데 필요하므로 바이알 어댑터를 바이알에 부착한 상태로 두십시오. 큰 루어 록 주사기를 부착할 준비가 될 때까지 희석제 주사기를 분리하지 마십시오.
- 별도의 큰 루어 록 주사기를 단단히 고정될 때까지 시계 방향으로 돌려 부착합니다.
- 플런저 로드를 천천히 당겨 용액을 주사기로 흡입합니다.
- 필요한 투여량을 얻기 위해 필요한 각 바이알에 대해 이 풀링 절차를 반복합니다. 풀링할 때는 다음 바이알(바이알 어댑터가 부착된 상태)에 부착할 준비가 될 때까지 큰 루어 록 주사기를 분리하지 마십시오. 필요한 투여량을 풀링한 후에는 큰 루어 록 주사기를 사용하여 투여를 진행하십시오.
2.3 투여
3 제형 및 함량
ELOCTATE는 바이알당 250, 500, 750, 1000, 1500, 2000, 3000, 4000, 5000 또는 6000 국제 단위(IU)를 함유하는 단일 용량 바이알에 백색에서 거의 백색의 동결 건조 분말로 제공됩니다. 실제 Factor VIII 역가는 각 ELOCTATE 바이알에 표시되어 있습니다.
4 금기 사항
ELOCTATE는 ELOCTATE 또는 그 부형제(수크로오스, 염화나트륨, L-히스티딘, 염화칼슘 및 폴리소르베이트 20)에 대해 생명을 위협하는 과민 반응을 경험한 적이 있는 환자에게는 금기입니다.
5 경고 및 주의 사항
5.1 과민 반응
ELOCTATE와 관련하여 과민 반응이 보고되었습니다. 아나필락시스를 포함한 알레르기 유형의 과민 반응이 제8인자 대체 제품과 관련하여 보고되었습니다. 아나필락시스로 진행될 수 있는 과민 반응의 초기 징후에는 안지오에데마, 흉부 압박감, 호흡 곤란, 천명, 두드러기 및 가려움증이 포함될 수 있습니다. 과민 반응이 발생하면 즉시 투여를 중단하고 적절한 치료를 시작하십시오.
5.2 중화 항체
ELOCTATE 투여 후 제8인자에 대한 중화 항체(억제제) 형성이 보고되었습니다. 적절한 임상 관찰 및 실험실 검사를 통해 모든 환자에서 제8인자 억제제 발생 여부를 모니터링하십시오. 혈장 제8인자 수치가 예상대로 증가하지 않거나 ELOCTATE 투여 후 출혈이 조절되지 않으면 억제제(중화 항체)가 존재할 가능성을 의심하십시오 [경고 및 주의 사항 (5.5) 참조].
5.4 카테터 관련 합병증
중심 정맥 접근 장치(CVAD)가 필요한 경우 국소 감염, 균혈증 및 카테터 부위 혈전증을 포함한 CVAD 관련 합병증 위험을 고려해야 합니다 [부작용 (6) 참조].
5.5 실험실 검사 모니터링
검증된 검사(예: 단일 단계 응고 검사)를 수행하여 혈장 제8인자 활성을 모니터링하여 적절한 제8인자 수치가 달성되고 유지되었는지 확인하십시오 [투여 방법 및 용량 (2) 참조].
제8인자 억제제 발생 여부를 모니터링하십시오. 예상 제8인자 혈장 수치가 달성되지 않거나 예상 ELOCTATE 용량으로 출혈이 조절되지 않으면 Bethesda 억제제 검사를 수행하십시오. Bethesda 단위(BU)를 사용하여 억제제 수치를 보고하십시오.
6 부작용
이전에 치료받은 환자(PTPs)의 임상 시험에서 보고된 가장 흔한 부작용(발생률 >0.5%)은 관절통, 권태감, 근육통, 두통 및 발진이었습니다. 이전에 치료받지 않은 환자(PUPs)의 임상 시험에서 보고된 가장 흔한 부작용(발생률 ≥1.0%)은 VIII 인자 억제, 기기 관련 혈전증 및 구진성 발진이었습니다.
6.1 임상 시험 경험
임상 시험은 매우 다양한 조건에서 수행되므로 한 약물의 임상 시험에서 관찰된 부작용 발생률을 다른 약물의 임상 시험에서 관찰된 발생률과 직접 비교할 수 없으며 실제로 관찰된 발생률을 반영하지 않을 수도 있습니다.
이전에 치료받은 환자(PTPs)
ELOCTATE는 중증 A형 혈우병(내인성 FVIII 활성도 <1% 또는 중증 A형 혈우병과 일치하는 유전적 돌연변이)이 있는 이전에 치료받은 환자(PTPs) 276명을 대상으로 한 5건의 완료된 연구에서 평가되었으며, 이 환자들은 루틴 예방 요법, 출혈 에피소드의 필요에 따른 치료 또는 수술 전 관리의 일환으로 ELOCTATE를 최소한 1회 투여받았습니다. 69명(25.0%)은 12세 미만의 소아였고, 25명(9.1%)은 청소년(12세 이상 18세 미만)이었으며, 182명(65.9%)은 성인(18세 이상)이었습니다. 200명의 환자가 최소 104주 동안 치료를 받았고, 151명의 환자가 최소 156주 동안 치료를 받았으며, 107명의 환자가 최소 208주 동안 치료를 받았습니다. 총 노출 일수(EDs)는 80,848일이었으며, 환자별 중앙값은 294일(범위 1-735일)이었습니다. 환자들은 총 82,024회 주사를 맞았으며, 환자별 ELOCTATE 주사의 중앙값은 303.5회(범위 1-755회)였습니다. 총 893.72 환자-년 동안 이상 사례(AEs)를 모니터링했습니다. 심혈관 위험 요인이 있는 2명의 환자(총 276명 중 0.7%)가 연구 중 심근 경색의 중대한 이상 반응을 경험했습니다.
루틴 예방 요법 또는 에피소드(필요에 따른) 요법으로 치료받은 276명 중 11명(4.0%)에서 이상 반응(ARs)이 보고되었습니다. 소아 환자와 성인 환자 간에 ARs에서 연령별 차이가 관찰되지 않았습니다. 표 3은 PTPs에서 가장 흔하게 발생하는 이상 반응을 요약한 것입니다. 단일 환자에서 각각 발생한 추가 이상 반응(발생률 0.4%)은 현기증, 미각 이상, 서맥, 고혈압, 홍조, 혈관병증(조사자 용어: 연구 약물 주사 후 혈관 통증), 기침, 하복부 통증, 요통, 관절 부종, 흉통, 추위 느낌, 열감 및 절차적 저혈압입니다. 2명의 환자가 발진과 관절통의 이상 반응으로 인해 연구에서 제외되었습니다. 연구에서 억제제는 검출되지 않았으며 아나필락시스 사례는 보고되지 않았습니다.
이전에 치료받지 않은 환자(PUPs)
ELOCTATE의 안전성은 중증 A형 혈우병(<1% 내인성 FVIII 활성)이 있는 103명의 피험자를 대상으로 한 완료된 한 연구(PUPs 연구)에서도 평가되었습니다. 전반적으로 치료 기간의 중앙값은 64.24주(범위: 0.0–206.8주)였습니다. 적어도 10일의 노출 일수(ED)를 가진 피험자 수는 87명(84.5%), 적어도 20 ED는 85명(82.5%), 적어도 50 ED는 81명(78.6%)이었습니다.
ELOCTATE로 루틴 예방, 일시적 또는 면역 관용 유도(ITI) 치료를 받은 103명 중 29명(28.2%)에서 부작용(ADR)이 보고되었습니다. PUPs의 ADR은 표 4에 요약되어 있습니다.
면역원성
임상 시험 피험자는 VIII 인자에 대한 중화 항체를 모니터링했습니다. PTPs는 VIII 인자에 대한 확인된 중화 항체를 개발하지 않았습니다. 25세의 한 피험자는 14주차에 0.73 BU의 일시적인 양성 중화 항체를 보였지만, 18일 후 반복 검사에서 확인되지 않았고 그 이후로도 확인되지 않았습니다.
PUPs 연구에서 중화 항체(억제제)의 발달이 28명의 피험자에서 관찰되었으며, 그 중 14명은 고역가 억제제를 가졌습니다. 노출 일수(ED) 마일스톤 이후 억제제 검사를 받은 피험자 또는 연구 기간 동안 언제든지 억제제를 개발한 피험자를 기준으로 VIII 인자 억제제 발달의 발생률은 다음과 같았습니다.
- 적어도 10 ED를 가진 90명의 피험자 중 28명(31.1%)
- 적어도 50 ED를 가진 86명의 피험자 중 28명(32.6%)
28명의 피험자에서 억제제 발달까지의 중앙값은 9 ED(사분위수 범위: 6.5–12)였습니다.
VIII 인자에 반응하는 항체의 검출은 검사의 민감도 및 특이성, 샘플 취급, 샘플 수집 시기, 동반 약물 및 기저 질환을 포함한 여러 요인에 크게 의존합니다. 따라서 ELOCTATE에 대한 항체 발생률을 다른 제품에 대한 항체 발생률과 비교하는 것은 오해의 소지가 있을 수 있습니다.
6.2 시판 후 경험
ELOCTATE의 시판 후 사용 중 다음과 같은 부작용이 확인되었습니다. 이러한 반응은 불확실한 규모의 모집단에서 자발적으로 보고되기 때문에, 항상 그 빈도를 신뢰할 수 있게 추정하거나 약물 노출과의 인과 관계를 확립할 수 있는 것은 아닙니다.
혈액 및 림프계 장애: VIII 인자 억제제 발달
면역 체계 장애: 과민 반응
8 특정 인구 집단에서의 사용
8.1 임신
위험 요약
임산부에서 ELOCTATE 사용에 대한 약물 관련 위험을 알려주는 연구는 없습니다. 지정된 인구 집단에서 주요 선천적 기형 및 유산의 배경 위험은 알려져 있지 않습니다. 그러나 미국 일반 인구에서 주요 선천적 기형의 배경 위험은 2-4%이고 유산은 임상적으로 인식된 임신의 15-20%입니다.
ELOCTATE를 사용한 동물 생식 및 발달 독성 연구는 수행되지 않았습니다. 태반 이동 연구에서 ELOCTATE는 임신 쥐에 20~50 IU/kg ELOCTATE의 임상 용량의 260~650배를 투여한 후 3~4시간 후에 쥐 태아 혈액 샘플에서 모체 혈액 수준의 약 1%(범위 0.2%~1.9%)로 검출되었습니다. [데이터 참조].
임산부에게 ELOCTATE를 투여했을 때 태아에게 해를 끼칠 수 있는지, 또는 생식 능력에 영향을 미칠 수 있는지 여부는 알려져 있지 않습니다. 임산부에게 ELOCTATE가 분명히 필요한 경우, 모체와 태아에 대한 위험이 알려져 있지 않다는 것을 환자에게 알려야 합니다.
동물 데이터
유전적으로 변형된 FVIII 결핍 쥐(Hem A 쥐) 임신 쥐에게 임신 말기인 임신 19일에 400 IU(약 13,000 IU/kg) ELOCTATE를 단회 정맥 주사했습니다. 투여 후 3~4시간 후에 모체 쥐와 태아에서 혈액 샘플을 채취하여 FVIII 활성을 FVIII 크로모젠 분석법을 사용하여 모체 및 태아 혈장에서 모두 측정했습니다. 임신한 HemA 쥐에 ELOCTATE를 투여한 후 태아 혈액의 FVIII 활성은 모체 혈액 수준의 약 1%였으며, 이는 ELOCTATE의 태반 이동이 발생할 수 있음을 시사합니다. 이러한 데이터의 인간에 대한 관련성은 알려져 있지 않습니다.
8.4 소아 사용
안전성 및 유효성 연구는 ELOCTATE를 최소 1회 이상 투여받은 18세 미만의 이전에 치료받은 소아 환자(PTPs) 82명(일상적인 예방, 출혈 에피소드의 필요에 따른 치료 또는 수술 전 관리의 일부로)에서 수행되었습니다. 청소년 대상은 성인 및 청소년 안전성 및 유효성 시험에 등록되었고, 12세 미만의 대상은 소아 시험에 등록되었습니다. ELOCTATE의 안전성 및 유효성은 한 연구(PUPs 연구)에서 6세 미만의 이전에 치료받지 않은 소아 환자(PUPs) 103명(중앙값 0.58년; 범위: 0.02~4년)에서 평가되었습니다. [부작용(6) 참조].
12세 미만의 평가 가능한 대상 54명을 대상으로 한 소아 연구의 약동학적 데이터는 6세 이상 환자에게는 용량 조절이 필요하지 않음을 보여주었습니다. 1~5세 어린이는 반감기가 짧고 클리어런스가 높았습니다(체중 조정). 따라서 이 연령대에서는 더 높은 용량 또는 더 빈번한 투여가 필요할 수 있습니다. [임상 약리학(12.3) 참조].
11 설명
ELOCTATE, 항혈우인자 (재조합), Fc 융합 단백질은 정맥 주사용으로 재구성하기 위한 무균성, 비발열성, 백색에서 벗어난 백색의 동결 건조 분말입니다. 이 제품은 250, 500, 750, 1000, 1500, 2000 3000, 4000, 5000 또는 6000 국제 단위 (IU)의 명목상 역가를 포함하는 단일 용량 바이알로 제공됩니다. ELOCTATE 바이알은 IU로 실제 함량이 표시되어 있습니다. 주사용 분말은 무균성 사전 충전 주사기로 제공되는 3mL의 무균성 주사용수 (SWFI)로 재구성됩니다. 재구성된 용액은 입자가 거의 없어야 합니다. 최종 제품에는 수크로스, 염화나트륨, L-히스티딘, 염화칼슘 및 폴리소르베이트 20과 같은 부형제가 포함되어 있습니다. ELOCTATE에는 방부제가 포함되어 있지 않습니다.
B-도메인 삭제 재조합 VIII 인자, Fc 융합 단백질 (BDD-rFVIIIFc)은 ELOCTATE의 활성 성분입니다. BDD-rFVIIIFc는 인간 면역 글로불린 G1 (IgG1) Fc 도메인 서열에 공유 결합된 인간 응고 인자 VIII의 B-도메인 삭제 유사체로 구성된 재조합 단백질입니다. 분자의 VIII 인자 부분은 90kDa의 중쇄와 80kDa의 경쇄 (내인성 VIII 인자와 유사)를 가지고 있으며, 이는 중앙 B-도메인의 14개 (908개 중) 아미노산으로 연결됩니다. FVIII 부분은 내인성 VIII 인자와 비교할 수 있는 번역 후 변형을 가지고 있습니다. 분자의 Fc 도메인은 IgG1의 힌지, CH2 및 CH3 영역을 포함합니다. BDD-rFVIIIFc는 겉보기 분자량이 220kDa인 1890개의 아미노산을 포함합니다. 발현된 단백질의 대부분은 단백질 분해적으로 두 개의 사슬 분자로 처리되지만, ELOCTATE에는 단일 사슬, 비처리 형태가 최대 39% 포함될 수도 있습니다. 두 분자 모두 VIII 인자 활성이 비슷한 것으로 나타났습니다.
BDD-rFVIIIFc는 광범위하게 특성화된 인간 배아 신장 (HEK) 세포주에서 재조합 DNA 기술로 생산됩니다. HEK 세포주는 동물 또는 인간 유래 단백질을 포함하지 않는 정의된 세포 배양 배지로 BDD-rFVIIIFc를 발현합니다. BDD-rFVIIIFc는 효모 발현 시스템에서 생산된 재조합 단일 사슬 항체 단편을 사용한 친화성 포획을 포함한 일련의 크로마토그래피 단계를 사용하여 정제됩니다. 정제 또는 제형 공정에는 인간 또는 동물 유래 단백질이 사용되지 않습니다. 생산 공정에는 바이러스 불활성화를 위한 세척제 처리 단계와 바이러스 제거를 위한 15nm 여과 단계라는 두 가지 전용 바이러스 제거 단계가 포함됩니다.
12 임상 약리학
12.1 작용 기전
ELOCTATE는 효과적인 지혈에 필요한 결손된 응고 인자 VIII을 일시적으로 대체하는 재조합 융합 단백질입니다. ELOCTATE는 인간 면역 글로불린 G1 (IgG1)의 Fc 영역을 포함하고 있으며, 이는 신생아 Fc 수용체 (FcRn)에 결합합니다. FcRn은 면역 글로불린의 리소좀 분해를 지연시켜 순환으로 다시 순환시키고 혈장 반감기를 연장하는 자연 발생 경로의 일부입니다.
12.2 약력학
혈우병 A는 기능적 응고 인자 VIII의 결핍을 특징으로 하는 출혈 장애로, 활성화 부분 트롬보플라스틴 시간 (aPTT) 검사로 측정한 환자 혈장 응고 시간이 연장됩니다. ELOCTATE로 치료하면 유효한 투여 기간 동안 aPTT가 정상화됩니다.
12.3 약동학
ELOCTATE (rFVIIIFc)의 약동학 (PK)은 28명의 피험자에서 50 IU/kg의 단일 용량을 10분 동안 정맥 주입한 후 평가되었습니다. PK 매개변수는 단일 단계 응고 검사로 측정한 혈장 FVIII 활성을 기반으로 했습니다. 반복 투여 후 14주에 얻은 PK 프로파일은 첫 번째 용량 투여 후 얻은 PK 프로파일과 유사했습니다. PK 데이터는 ELOCTATE가 연장된 순환 반감기를 갖는다는 것을 보여줍니다. 1%까지의 시간은 5.10일 (95% CI: 4.54, 5.66)이었습니다. 현재 시판되는 재조합 인자 VIII (ADVATE®)와 비교했을 때 ELOCTATE의 말초 혈장 반감기는 1.5배 더 길었습니다.
소아 및 청소년 약동학
ELOCTATE의 약동학 (PK) 매개변수는 성인 및 청소년 연구에서 청소년 (12~17세)과 소아 연구에서 소아 (1~5세 및 6~11세)에 대해 결정되었습니다. 표 5는 18세 미만의 65명의 피험자에 대한 소아 데이터에서 50 IU/kg의 단일 용량을 투여한 후 계산된 PK 매개변수를 보여줍니다.
성인 및 청소년과 비교하여 체중 조정된 청소율은 1~5세 소아에서 75% 더 높았습니다. 이러한 결과는 1~5세 소아에서 용량 조정이 필요함을 나타냅니다.
6~17세 소아 피험자에 대한 PK 평가 결과, PK 프로파일과 PK 매개변수의 산술 평균이 성인과 유사한 것으로 나타났습니다. 따라서 6세 이상의 피험자는 연령 기반 용량 조정이 필요하지 않습니다.
| PK 매개변수* | 소아 연구 | 성인 및 청소년 연구 | ||
|---|---|---|---|---|
| 1~5세 | 6~11세 | 12~17세 | 성인† | |
| N=23 | N=31 | N=11 | N=28 | |
|
약어: CI = 신뢰 구간; AUC = FVIII 활성 시간 곡선 아래 면적; t1/2 = 말초 반감기; MRT = 평균 체류 시간; CL = 체중 조정된 청소율; Vss = 정상 상태에서 체중 조정된 분포 용적 |
||||
| 증분 회복 (IU/kg당 IU/dL) |
1.92 (1.80, 2.04) |
2.44 (2.07, 2.80) |
1.85 (1.58, 2.12) |
2.26 (2.13, 2.40) |
| AUC/용량 (IU/kg당 IU x h/dL) |
30.0 (26.5, 33.6) |
41.9 (34.0, 49.8) |
38.7 (34.3, 43.1) |
54.1 (47.0, 61.1) |
| t½ (h) | 12.7 (11.2, 14.1) |
14.9 (12.0, 17.8) |
16.4 (14.1, 18.6) |
19.7 (17.4, 22.0) |
| MRT (h) | 17.2 (15.4, 19.1) |
20.9 (17.1, 24.7) |
23.1 (19.9, 26.4) |
26.1 (23.2, 28.9) |
| CL (mL/h/kg) | 3.60 (3.13, 4.07) |
2.78 (2.44, 3.13) |
2.66 (2.34, 2.98) |
2.06 (1.78, 2.34) |
| Vss (mL/kg) | 58.6 (54.9, 62.3) |
52.1 (45.3, 59.0) |
60.3 (53.3, 67.3) |
49.5 (46.9, 52.2) |
13 비임상 독성학
13.1 발암성, 돌연변이 유발성, 생식능력 저해
ELOCTATE의 발암 효과를 조사한 장기 동물 연구는 수행되지 않았습니다. In vitro 및 in vivo에서 ELOCTATE의 돌연변이 유발성 또는 생식능력에 대한 영향을 조사하는 시험은 수행되지 않았습니다.
14 임상 연구
ELOCTATE의 안전성 및 유효성은 이전에 치료받은 환자(PTPs)(성인 및 청소년 연구 및 소아 연구)에서 다기관, 전향적, 공개 라벨 임상 시험 2건과 연장 연구에서 평가되었습니다.
성인 및 청소년 연구는 2가지 예방적 치료 요법(개별화 및 고정 주간)의 유효성을 일회성(요청 시) 치료와 비교했습니다. 출혈 에피소드 치료에서 지혈 효능을 결정했습니다. 그리고 주요 수술 절차를 받는 피험자의 수술 전 관리 중 지혈 효능을 결정했습니다. 이 연구에는 중증 혈우병 A(<1% 내인성 제8인자 활성 또는 중증 혈우병 A와 일치하는 유전적 돌연변이)를 가진 이전에 치료받은 남성 환자(PTPs) 165명이 등록되었습니다. 피험자의 연령은 12세에서 65세였으며, 여기에는 12세에서 17세 사이의 소아 피험자 13명이 포함되었습니다. 등록된 165명의 피험자 중 164명이 ELOCTATE를 최소 1회 투여받았고 163명(98%)이 유효성 평가 대상이었습니다. 총 153명의 피험자(93%)가 연구를 완료했습니다.
소아 연구는 개별화된 예방적 치료의 유효성을 평가했습니다. 출혈 에피소드 치료에서 지혈 효능을 결정했습니다. 그리고 수술 절차를 받는 피험자의 수술 전 관리 중 지혈 효능을 결정했습니다. 이 연구에는 중증 혈우병 A(<1% 내인성 FVIII 활성 또는 중증 혈우병 A와 일치하는 유전적 돌연변이)를 가진 이전에 치료받은 남성 소아 환자 71명이 등록되었습니다. 등록된 71명의 피험자 중 69명이 ELOCTATE를 최소 1회 투여받았고 유효성 평가 대상이었습니다. 모든 피험자는 12세 미만이었습니다(35명은 1세에서 5세 사이였고 34명은 6세에서 11세 사이였습니다).
연장 연구는 예방적 치료 요법 또는 요청 시 치료의 안전성 및 유효성을 평가했습니다. 그리고 수술 절차를 받는 피험자의 수술 전 관리 중 지혈 효능을 평가했습니다. 이 연구에는 성인 및 청소년 연구 또는 소아 연구를 완료한 중증 혈우병 A를 가진 이전에 치료받은 남성 환자(2세에서 66세) 240명이 등록되었습니다.
요청 시 치료 및 출혈 에피소드 조절
성인 및 청소년 연구에서 106명의 피험자에서 총 757건의 출혈 에피소드가 ELOCTATE로 치료되었습니다. 대부분의 출혈 에피소드는 자발적이었고 관절에 국한되었습니다. 출혈 에피소드 치료에 사용된 주입당 중간 용량은 27.35(IQR 22.73, 32.71) IU/kg였습니다. 각 주입에 대한 반응 평가는 피험자가 치료 후 8-12시간에 기록했습니다. 반응을 평가하기 위해 우수, 양호, 중간 및 반응 없음의 4점 등급 척도가 사용되었습니다. 12세 이상 피험자의 출혈 에피소드 조절 효능은 표 6에 요약되어 있습니다.
| 새로운 출혈 에피소드 | (n=757) | |
|---|---|---|
|
||
| 출혈 에피소드 치료를 위한 주입 횟수 | ||
| 1회 주입 | 661 (87.3%) | |
| 2회 주입 | 79 (10.4%) | |
| >2회 주입 | 17 (2.2%) | |
| 첫 번째 주입에 대한 반응* | (n=745) | |
| 우수 또는 양호 | 78.1% | |
| 중간 | 21.2% | |
| 반응 없음 | 0.7% | |
소아 연구에서, 69명의 소아 피험자에서 총 86건의 출혈 에피소드가 ELOCTATE로 치료되었습니다. 각 주입에 대한 반응 평가는 치료 후 8~12시간에 피험자에 의해 기록되었습니다. 반응을 평가하기 위해 우수, 양호, 중간 및 반응 없음의 4점 등급 척도가 사용되었습니다. 12세 미만 피험자에서 출혈 에피소드 조절의 효능은 표 7에 요약되어 있습니다.
모든 평가 가능한 첫 번째 주입의 경우 출혈 치료에서 지혈 효능은 우수 또는 양호로 평가되었습니다.
| 1-5세
(n=35) |
6~11세
(n=34) |
총계 (<12세) (n=69) |
||
|---|---|---|---|---|
|
||||
| 새로운 출혈 에피소드 | (n=38) | (n=48) | (n=86) | |
| 출혈 에피소드 치료를 위한 주입 횟수 | 1회 주입 | 29 (76.3%) | 41 (85.4%) | 70 (81.4%) |
| 2회 주입 | 7 (18.4%) | 3 (6.3%) | 10 (11.6%) | |
| >2회 주입 | 2 (5.3%) | 4 (8.3%) | 6 (7.0%) | |
| 출혈 에피소드 치료를 위한 주입 당 중간 용량 (IU/kg) (IQR) | 51.35 (29.94, 59.52) |
48.15 (29.08, 55.97) |
49.69 (29.41, 56.82) |
|
| 출혈 에피소드 치료를 위한 중간 총 용량 (IU/kg) (IQR) | 56.40 (29.94, 72.46) |
53.49 (29.08, 66.80) |
54.90 (29.41, 71.09) |
|
| 첫 번째 주입에 대한 반응* | (n=35) | (n=46) | (n=81) | |
| 우수 또는 양호 | 32 (91.4%) | 43 (93.5%) | 75 (92.6%) | |
| 중간 | 3 (8.6%) | 1 (2.2%) | 4 (4.9%) | |
| 반응 없음 | 0 (0.0%) | 2 (4.3%) | 2 (2.5%) | |
주요 수술
성인 및 청소년 연구 및 연장 연구에서 32명의 피험자에 대한 45건의 수술에서 지혈을 평가했습니다. 소아 연구 또는 약동학 연구에서는 주요 수술이 없었습니다. 45건의 주요 수술 중 36건(80.0%)은 지혈을 유지하기 위해 수술 전후 단일 투여가 필요했습니다. 최소한 한 번의 투여로 치료받은 42건의 주요 수술에서 수술 중 지혈을 유지하기 위한 주입당 중간 평균 투여량은 59.1 IU/kg(범위 35-111)이었습니다. 수술 당일 대부분의 피험자는 두 번째 주입을 받았습니다. 수술 당일 총 투여량은 37.6-157.9 IU/kg였습니다.
지혈 반응은 연구자에 의해 다음과 같은 순서척도를 사용하여 평가되었습니다.
우수: 수술 중 및 수술 후 혈액 손실이 비혈우병 환자와 유사하거나 적습니다. rFVIIIFc의 추가 투여가 필요하지 않으며 혈액 성분 수혈 요구량은 비혈우병 환자와 유사합니다.
양호: 수술 중 및/또는 수술 후 출혈이 비혈우병 환자에 대한 예상치보다 약간 증가했지만 차이가 임상적으로 유의하지 않았습니다. 수술 중 혈액 손실은 비혈우병 환자에 대한 예상치보다 250mL를 초과하지 않았으며 rFVIIIFc의 추가 투여가 필요하지 않았으며 혈액 성분 수혈 요구량은 비혈우병 환자와 유사합니다.
보통: 수술 중 및/또는 수술 후 혈액 손실이 비혈우병 환자에 대한 예상치보다 증가했으며 추가 치료가 필요했습니다. 수술 중 혈액 손실은 혈우병이 없는 사람에 대한 예상치보다 250~500mL를 초과하거나 rFVIIIFc의 추가 투여가 필요하거나 혈액 성분 수혈 요구량이 증가했습니다.
불량/없음: 비혈우병 환자에 대한 예상치보다 상당히 증가한 수술 중 및/또는 수술 후 출혈이 개입을 요구했으며 혈우병 이외의 수술/의학적 문제로 설명되지 않았습니다. 수술 중 혈액 손실은 비혈우병 환자에 대한 예상치보다 500mL를 초과하거나 예상치 못한 저혈압 또는 출혈로 인한 예상치 못한 중환자실 이송 또는 혈액 성분 수혈 요구량이 상당히 증가했습니다.
29명의 피험자에 대한 41건의 주요 수술에서 지혈 반응을 평가한 결과 38건(93%)의 수술에서 우수, 3건(7%)의 수술에서 양호로 평가되었습니다.
평가된 수술 유형에는 관절 치환(양측 무릎, 단측 팔꿈치, 고관절 및 무릎 치환), 발목 유합 및 절단과 같은 주요 정형외과 수술이 포함됩니다. 기타 주요 수술에는 충수염 절제술, 관절경 수술, 척추 수술 및 서혜부 탈장 수술이 포함됩니다.
경미한 수술
3개 연구에서 59명의 피험자에 대한 72건의 경미한 수술 절차에 대한 지혈 평가를 실시한 결과, 모든 피험자(100%)가 우수 또는 양호한 반응을 보였습니다(우수 반응 [72건 중 61건; 84.7%] 및 양호 반응 [72건 중 11건; 15.3%]).
성인 및 청소년 연구
일상적인 예방의 효능은 필요에 따른 치료와 비교하여 평가되었습니다. 총 117명의 피험자가 개별화된 주 2회 요법을 받았으며, 첫날 25 IU/kg으로 시작하여 4일째 50 IU/kg으로 시작했습니다. 기저치보다 1%에서 3% 이상의 골 농도를 유지하거나 출혈을 예방하기 위해 임상적으로 지시된 경우 더 높은 범위 내에서 25-65 IU/kg을 3-5일마다 조정했습니다. 중간 투여 간격은 3.5일이었습니다. 최소 6개월 동안 치료받은 112명의 피험자 중 111명(99%)이 연구 마지막 3개월 동안 3일 이상의 투여 간격을 달성했고, 39명(35%)이 4일 이상의 투여 간격을 달성했으며, 33명(29%)이 5일 이상의 투여 간격을 달성했습니다. 23명의 피험자는 28주 동안 중간 기간 동안 주 1회 65 IU/kg의 ELOCTATE를 받았습니다. 추가로 23명의 피험자는 출혈 에피소드 치료를 위해 ELOCTATE를 간헐적으로(필요에 따라) 투여받았으며, 연구 기간은 중간 29주였습니다. 연간 출혈률(ABR)을 분석하기 위해 음의 이항 모델을 사용하여 개별화된 예방군의 피험자는 에피소드(필요에 따라)군에 비해 ABR이 92%(p<0.001) 통계적으로 유의하게 감소했고, 주 예방군의 피험자는 에피소드(필요에 따라)군에 비해 ABR이 76%(p<0.001) 통계적으로 유의하게 감소했습니다. 117명(45%) 중 53명의 피험자가 개별화된 예방을 받는 동안 출혈 에피소드를 경험하지 않았고, 23명 중 4명(17%)의 피험자가 주 예방을 받는 동안 출혈 에피소드를 경험하지 않았습니다.
효능 평가 대상 피험자의 중간 ABR은 표 8에 요약되어 있습니다.
소아 연구
69명의 피험자는 첫째 날 25 IU/kg, 넷째 날 50 IU/kg으로 구성된 주 2회 요법으로 시작하여 개별화된 예방적 용량 요법으로 ELOCTATE를 투여받았습니다. 용량은 기저치 대비 1% 이상의 최저치를 유지하거나 출혈을 예방하기 위해 임상적으로 필요에 따라 2일 간격으로 최소 투여 간격을 두고 25-80 IU/kg 범위 내에서 조정할 수 있었습니다. 중간 투여 간격은 3.49일(사분위수 범위, 3.46~3.51일)이었으며, 연령대 간에 중간 투여 간격에 차이가 없었습니다. 피험자의 89.9%가 주 2회 간격으로 유지되었습니다. 1~5세 피험자의 ELOCTATE 중간 주간 용량은 91.63 IU/kg(사분위수 범위(IQR), 84.72~104.56 IU/kg)이었습니다. 6~11세 연령대 피험자의 경우 중간 주간 용량은 86.88 IU/kg(IQR, 79.12~103.08 IU/kg)이었습니다.
모든 피험자 중 32명(46.4%)은 출혈 에피소드를 경험하지 않았습니다(1~5세 18명(51.4%), 6~11세 14명(41.2%)). 효능 평가가 가능한 중간 ABR의 제시는 표 9에 요약되어 있습니다.
15 참고 문헌
- Sommer JM, Moore N, McGuffie-Valentine B, et al. Comparative field study evaluating the activity of recombinant factor VIII Fc fusion protein in plasma samples at clinical haemostasis laboratories. Haemophilia. 2014;20:294–300.
16 공급/보관 및 취급 방법
공급 형태
ELOCTATE는 명목상 250, 500, 750, 1000, 1500, 2000, 3000, 4000, 5000 또는 6000 국제 단위(IU)의 Factor VIII 역가를 함유한 단회용 바이알, 3mL의 주사용 멸균수가 채워진 사전 충전 주사기 및 멸균 바이알 어댑터(재구성 장치)로 구성된 키트로 제공됩니다. 각 바이알의 라벨과 상자에는 IU로 표시된 ELOCTATE의 실제 양이 명시되어 있습니다.
천연 고무 라텍스로 만들어지지 않았습니다.
| 역가 | 역가 색상 코드 | 키트 NDC 번호 |
| 250 IU | 노란색 | 71104-801-01 |
| 500 IU | 빨간색 | 71104-802-01 |
| 750 IU | 자홍색 | 71104-803-01 |
| 1000 IU | 녹색 | 71104-804-01 |
| 1500 IU | 짙은 녹색 | 71104-805-01 |
| 2000 IU | 로열 블루 | 71104-806-01 |
| 3000 IU | 연한 회색 | 71104-807-01 |
| 4000 IU | 주황색 | 71104-808-01 |
| 5000 IU | 연한 갈색 | 71104-809-01 |
| 6000 IU | 보라색 | 71104-810-01 |
재구성 전:
- ELOCTATE 바이알을 빛으로부터 보호하기 위해 원래 포장 상태로 보관하십시오.
- ELOCTATE는 분말 형태로 2°C~8°C(36°F~46°F)에서 보관하십시오. 사전 충전 희석제 주사기를 손상시키지 않도록 냉동하지 마십시오.
- ELOCTATE는 라벨에 인쇄된 유효 기간 내에 최대 30°C(86°F)를 초과하지 않는 실온에서 최대 6개월 동안 단일 기간 동안 보관할 수 있습니다.
- 실온에서 보관하는 경우 제공된 영역에 상자에 ELOCTATE를 냉장 보관에서 꺼낸 날짜를 기록하십시오. 실온에서 보관한 후에는 제품을 냉장고에 다시 넣지 마십시오.
- 바이알에 인쇄된 유효 기간 또는 상자에 기록된 날짜로부터 6개월 후 중 더 빠른 날짜가 지나면 사용하지 마십시오.
재구성 후:
- 재구성된 제품은 최대 30°C(86°F)를 초과하지 않는 실온에서 최대 3시간 동안 보관할 수 있습니다. 직사광선을 피하십시오. 재구성 후 3시간 이내에 사용하지 않으면 폐기해야 합니다.
- 재구성된 용액이 흐리거나 입자가 있는 경우 ELOCTATE를 사용하지 마십시오.
- 사용하지 않은 ELOCTATE는 폐기하십시오.
17 환자 상담 정보
환자에게 다음과 같이 알려주십시오.
- FDA 승인 환자 라벨(환자 정보 및 사용 지침)을 읽으십시오.
- 과민 반응이 발생하면 즉시 의료 서비스 제공자에게 연락하거나 응급실로 가십시오. 과민 반응의 초기 징후에는 발진, 두드러기, 가려움증, 얼굴 부종, 가슴 답답함 및 천명이 포함될 수 있습니다.
- Factor VIII 치료에 대한 임상적 반응이 없는 경우 의료 서비스 제공자 또는 치료 시설에 연락하여 추가 치료 및/ 또는 평가를 받으십시오. 이는 억제제 발생의 징후일 수 있습니다.
제조사:
Bioverativ Therapeutics Inc.
Waltham, MA 02451
A SANOFI COMPANY
미국 라이선스 번호 2078
©2023 Bioverativ Therapeutics Inc. 모든 권리 보유.
ELOCTATE®는 Bioverativ Therapeutics Inc.의 등록 상표입니다.
특허 정보: https://www.sanofi.us/en/products-and-resources/patents
환자용 요약 정보
환자 정보
ELOCTATE® /el’ ok’ tate /
[항혈우인자 (재조합), Fc 융합 단백질]
ELOCTATE를 사용하기 전과 재충전할 때마다 이 환자 정보를 주의 깊게 읽어보십시오. 새로운 정보가 있을 수 있습니다. 이 환자 정보는 의료 서비스 제공자와 귀하의 의학적 상태 또는 치료에 대해 이야기하는 것을 대신할 수 없습니다.
ELOCTATE는 무엇입니까?
ELOCTATE는 혈우병 A(선천적 제 VIII 인자 결핍) 환자의 출혈을 조절하고 예방하는 데 도움이 되는 주사제입니다.
의료 서비스 제공자는 수술을 받을 때 ELOCTATE를 투여할 수 있습니다.
누가 ELOCTATE를 사용해서는 안 됩니까?
과거에 ELOCTATE에 알레르기 반응이 있었던 경우 ELOCTATE를 사용해서는 안 됩니다.
ELOCTATE를 사용하기 전에 의료 서비스 제공자에게 무엇을 알려야 합니까?
다음 사항에 대해 의료 서비스 제공자와 상담하십시오.
- 현재 또는 과거에 앓고 있는 모든 의학적 문제.
- 복용하는 모든 처방약과 비처방약, 의약품, 보충제 또는 허브 약초를 포함하여.
- 임신 중이거나 임신을 계획하고 있는 경우. ELOCTATE가 태아에게 해를 끼칠 수 있는지 여부는 알려져 있지 않습니다.
- 모유 수유. ELOCTATE가 모유로 전달되는지 여부와 아기에게 해를 끼칠 수 있는지 여부는 알려져 있지 않습니다.
ELOCTATE는 어떻게 사용해야 합니까?
ELOCTATE는 정맥 주입으로 투여됩니다. 의료 서비스 제공자는 스스로 주입하는 방법을 알려주고, 처음 ELOCTATE를 투여할 때는 지켜볼 수 있습니다.
ELOCTATE를 사용한 후에도 출혈이 조절되지 않으면 즉시 의료 서비스 제공자에게 연락하십시오.
ELOCTATE의 가능한 부작용은 무엇입니까?
ELOCTATE에 알레르기 반응이 나타날 수 있습니다. 호흡 곤란, 가슴 답답함, 얼굴 부종, 발진 또는 두드러기가 나타나면 즉시 의료 서비스 제공자 또는 응급실에 연락하십시오.
신체는 ELOCTATE에 대한 항체인 “억제제”를 생성할 수도 있습니다. 이는 ELOCTATE가 제대로 작동하지 못하게 할 수 있습니다. 의료 서비스 제공자는 억제제를 확인하기 위해 혈액 검사를 실시할 수 있습니다.
ELOCTATE의 추가적인 흔한 부작용으로는 두통, 발진, 관절통, 근육통 및 전반적인 불편함이 있습니다.
체내에 삽입된 정맥 카테터와 같이 비정상적인 혈액 응고 위험 요소가 있는 경우 제 VIII 인자 치료는 이러한 위험을 증가시킬 수 있습니다.
이것들은 ELOCTATE의 가능한 부작용의 전부가 아닙니다. 귀찮거나 사라지지 않는 부작용이 있으면 의료 서비스 제공자에게 알리십시오.
ELOCTATE는 어떻게 보관해야 합니까?
- ELOCTATE를 원래 포장에 보관하십시오.
- 빛으로부터 보호하십시오.
- 냉동하지 마십시오.
- 냉장 보관(2°C~8°C 또는 36°F~46°F)하거나 실온(30°C(86°F) 이하)에서 최대 6개월 동안 보관하십시오.
- 실온 보관 시:
- –
- 제품을 냉장 보관에서 꺼낸 날짜를 상자에 적어 두십시오.
- –
- 이 6개월 기간이 끝나기 전에 제품을 사용하거나 폐기하십시오.
- –
- 제품을 냉장고에 다시 넣지 마십시오.
바이알에 인쇄된 유효 기간 또는 냉장 보관에서 꺼낸 경우 상자에 적힌 날짜 중 더 빠른 날짜가 지난 후에는 ELOCTATE를 사용하지 마십시오.
재구성(희석액과 혼합) 후:
- 재구성된 용액이 투명하거나 약간 불투명하고 무색이 아니면 ELOCTATE를 사용하지 마십시오.
- 재구성된 제품을 가능한 한 빨리 사용하십시오.
- 재구성된 용액은 실온(30°C(86°F) 이하)에서 최대 3시간 동안 보관할 수 있습니다. 재구성된 제품을 직사광선으로부터 보호하십시오. 3시간 이내에 사용하지 않은 제품은 폐기하십시오.
ELOCTATE에 대해 알아야 할 다른 사항은 무엇입니까?
의약품은 때때로 여기에 나열된 목적 이외의 목적으로 처방됩니다. ELOCTATE를 처방받지 않은 질환에 사용하지 마십시오. ELOCTATE를 다른 사람과 공유하지 마십시오. 다른 사람이 귀하와 같은 증상을 보이더라도 마찬가지입니다.
이 환자 정보는 미국 식품의약국(FDA)의 승인을 받았습니다.
제조사:
Bioverativ Therapeutics Inc.
Waltham, MA 02451
A SANOFI COMPANY
미국 라이선스 번호 2078
©2023 Bioverativ Therapeutics Inc. 모든 권리 보유.
ELOCTATE®는 Bioverativ Therapeutics Inc.의 등록 상표입니다.
개정: 2023년 5월
사용 지침
ELOCTATE®
Antihemophilic Factor (Recombinant), Fc Fusion Protein
INSTRUCTIONS FOR USE
ELOCTATE를 사용하기 전과 재충전할 때마다 사용 설명서를 읽으십시오. 새로운 정보가 있을 수 있습니다. 이 정보는 의료 서비스 제공자와 귀하의 의학적 상태 또는 치료에 대해 이야기하는 것을 대신하지 않습니다.
의료 서비스 제공자가 ELOCTATE를 처음 사용할 때 ELOCTATE를 재구성하고 투여하는 방법을 귀하 또는 보호자에게 보여주어야 합니다.
ELOCTATE 키트의 유효 기간을 확인하십시오.
사용하지 마십시오 유효 기간이 지난 제품.
ELOCTATE 바이알과 희석제를 실온으로 가져오십시오.
사용하지 마십시오 바이알과/또는 희석제를 뜨거운 물에 넣는 것과 같이 외부 열원을 사용합니다.
깨끗하고 평평한 작업대를 찾고 ELOCTATE를 재구성하고 투여하는 데 필요한 모든 용품을 모으십시오.
비누와 물로 손을 씻으십시오. 무균 기법 (깨끗하고 세균이 없는)을 사용해야 합니다.
키트 구성:
재구성
POOLING
POOLING은 정맥 주입 전에 재구성된 바이알 2개 이상을 더 큰 주사기에(희석제 주사기가 아닌) 합치는 과정입니다.
바이알을 2개 이상 사용하는 경우 다음 pooling 단계를 따르십시오.
큰 루어 록 주사기를 부착하는 데 필요하므로 바이알 어댑터를 바이알에 부착한 상태로 두십시오.
다음 바이알(바이알 어댑터 부착)에 큰 루어 록 주사기를 부착할 준비가 될 때까지 희석제 주사기 또는 큰 루어 주사기를 분리하지 마십시오.
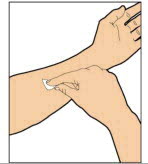
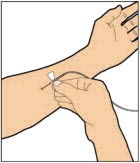
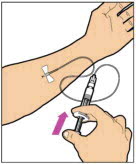
투여 (정맥 주사)
ELOCTATE는 약물 분말을 희석제로 재구성한 후 정맥 주입으로 투여합니다.
의료 서비스 제공자는 ELOCTATE를 주입하는 방법을 알려줄 것입니다. 자가 주입 방법을 익힌 후에는 다음 지침을 따르십시오.
재구성된 ELOCTATE에 입자가 보이거나 변색되었거나 흐리면 투여하지 마십시오.
보관 조건 – 제품 키트
사용할 때까지 냉장 보관하십시오.
직사광선을 피하십시오.
보관 조건 – 재구성
ELOCTATE는 재구성 후 3시간 이내에 투여해야 합니다.
재구성 후에는 냉장 보관하지 마십시오.
직사광선을 피하십시오.
이 사용 지침은 미국 식품의약국(FDA)의 승인을 받았습니다.
제조사:
Bioverativ Therapeutics Inc.
Waltham, MA 02451
A SANOFI COMPANY
미국 라이선스 번호 2078
©2023 Bioverativ Therapeutics Inc. 판권 소유.
자세한 내용은 www.ELOCTATE.com을 방문하거나 1-855-693-5628로 전화하십시오.
2023년 5월 개정
주요 표시 패널 – 키트 상자 – 250 IU
250 IU 명목
NDC 71104-801-01
단일 용량 바이알 1개
3mL 사전 충전
희석제 주사기 포함
ELOCTATE®
혈우병 인자
(재조합), Fc 융합 단백질
정맥 주사용
처방전에 의해서만 구입 가능
제조사:
Bioverativ Therapeutics Inc.
Waltham, MA 02451
미국 허가 번호 2078
www.ELOCTATE.com
Bioverativ

주요 표시 패널 – 키트 상자 – 500 IU
500 IU 명목
NDC 71104-802-01
단일 용량 바이알 1개
3mL 사전 충전
희석제 주사기 포함
ELOCTATE®
혈우병 인자
(재조합), Fc 융합 단백질
정맥 주사용
처방전에 의해서만 구입 가능
제조사:
Bioverativ Therapeutics Inc.
Waltham, MA 02451
미국 라이선스 번호 2078
www.ELOCTATE.com
Bioverativ

주요 표시 패널 – 키트 상자 – 750 IU
750 IU 명목
NDC 71104-803-01
단일 용량 바이알 1개
3mL 사전 충전
희석제 주사기 포함
ELOCTATE®
혈우병 인자
(재조합), Fc 융합 단백질
정맥 주사용
처방전에 의해서만 구입 가능
제조사:
Bioverativ Therapeutics Inc.
Waltham, MA 02451
미국 허가 번호 2078
www.ELOCTATE.com
Bioverativ

주요 표시 패널 – 키트 상자 – 1000 IU
1000 IU 명목
NDC 71104-804-01
단일 용량 바이알 1개
3mL 사전 충전
희석제 주사기 포함
ELOCTATE®
혈우병 인자
(재조합), Fc 융합 단백질
정맥 주사용
처방전에 의해서만 구입 가능
제조사:
Bioverativ Therapeutics Inc.
Waltham, MA 02451
미국 라이선스 번호 2078
www.ELOCTATE.com
Bioverativ

주요 표시 패널 – 키트 상자 – 1500 IU
1500 IU 명목
NDC 71104-805-01
단일 용량 바이알 1개
3mL 사전 충전
희석제 주사기 포함
ELOCTATE®
항혈우인자
(재조합), Fc 융합 단백질
정맥 주사용
처방전 의약품
제조사:
Bioverativ Therapeutics Inc.
Waltham, MA 02451
미국 허가 번호 2078
www.ELOCTATE.com
Bioverativ

주요 표시 패널 – 키트 상자 – 2000 IU
2000 IU 명목
NDC 71104-806-01
단일 용량 바이알 1개
3mL 사전 충전
희석제 주사기 포함
ELOCTATE®
혈우병 인자
(재조합), Fc 융합 단백질
정맥 주사용
처방전에 의해서만 구입 가능
제조사:
Bioverativ Therapeutics Inc.
Waltham, MA 02451
미국 허가 번호 2078
www.ELOCTATE.com
Bioverativ

주요 표시면 – 키트 상자 – 3000 IU
3000 IU Nominal
NDC 71104-807-01
3mL 사전 충전형
희석액 주사기가 들어 있는
일회용 바이알 1개
ELOCTATE®
Antihemophilic Factor
(Recombinant), Fc Fusion Protein
정맥 주사용
처방전 전용
제조:
Bioverativ Therapeutics Inc.
Waltham, MA 02451
미국 라이선스 번호 2078
www.ELOCTATE.com
Bioverativ

주요 표시면 – 키트 상자 – 4000 IU
공칭 4000 IU
NDC 71104-808-01
3mL 사전 충전형
희석액 주사기가 들어 있는
일회용 바이알 1개
ELOCTATE®
Antihemophilic Factor
(Recombinant), Fc Fusion Protein
정맥 주사용
처방전에 의해서만 판매
제조:
Bioverativ Therapeutics Inc.
Waltham, MA 02451
미국 라이선스 번호 2078
www.ELOCTATE.com
Bioverativ

주요 표시 패널 – 키트 상자 – 5000 IU
5000 IU 명목
NDC 71104-809-01
단일 용량 바이알 1개
3mL 사전 충전
희석제 주사기 포함
ELOCTATE®
혈우병 인자
(재조합), Fc 융합 단백질
정맥 주사용
처방전에 의해서만 구입 가능
제조사:
Bioverativ Therapeutics Inc.
Waltham, MA 02451
미국 라이선스 번호 2078
www.ELOCTATE.com
Bioverativ

주요 표시 패널 – 키트 상자 – 6000 IU
6000 IU 명목
NDC 71104-810-01
단일 용량 바이알 1개
3mL 사전 충전
희석제 주사기 포함
ELOCTATE®
항혈우인자
(재조합), Fc 융합 단백질
정맥 주사용
처방전에 의해서만 구입 가능
제조사:
Bioverativ Therapeutics Inc.
Waltham, MA 02451
미국 허가 번호 2078
www.ELOCTATE.com
Bioverativ